Versión 1 - 5/09/22
En prevención primaria de cáncer colorrectal, la evidencia disponible sugiere un beneficio del uso de ácido acetilsalicílico (ASA). Sin embargo, el efecto es evidente sólo después de más de 10 años de uso continuo y conlleva mayor riesgo de sangrados clínicamente importantes. Por tanto, se podría usar en prevención primaria de cáncer colorrectal en pacientes con mayor riesgo (factores hereditarios o lesiones premalignas) o como indicación adicional por prevención cardiovascular, balanceando el riesgo con las preferencias del paciente.
Certeza de la evidencia: muy baja para incidencia y mortalidad por cáncer colorrectal, baja para los desenlaces de seguridad (sangrado) por riesgo de sesgo, imprecisión y evidencia indirecta.
Otro mensaje clave:
- Es esperable que el efecto preventivo se observe en pacientes que reciben ASA por otra indicación, si la duración del tratamiento es suficiente.
Buena práctica clínica
Se debe promover el control de factores de riesgo modificables para cáncer colorrectal: suspender el consumo de cigarrillo y alcohol, controlar peso, evitar dietas bajas en fibra o ricas en grasas, entre otros.
Es importante saber lo que no se conoce
Se desconoce la influencia de factores de riesgo modificables y no modificables en el efecto preventivo del ASA en cáncer colorrectal.
Antecedentes
En Colombia y el mundo, el cáncer colorrectal (CCR) es el tercer tipo más frecuente (1-3). En nuestro país, entre 2019 y 2020 se reportaron 23 000 casos (15% nuevos) y ocurrieron 2 384 fallecimientos a causa de la enfermedad. Para 2020 la incidencia fue de 6.94, la prevalencia de 47.57 y la mortalidad de 4.96 casos por cada 100 000 habitantes, representando un aumento de 51% en la incidencia y 23% en la prevalencia (1). Además, la Cuenta de Alto Costo menciona que 27% de los casos no son estadificados oportunamente (1). El aumento en la incidencia y las brechas de diagnóstico persistentes, ponen de manifiesto la importancia de establecer estrategias de prevención y detección temprana de la enfermedad.
Una de estas posibilidades sería el uso de ASA, un inhibidor de la cicloxigenasa (COX) 1 y 2, que resulta en una acción analgésica, antiinflamatoria y antiagregante plaquetaria (4). Por este último beneficio, es ampliamente usada en prevención secundaria de eventos cardiovasculares (5) e incluso se ha propuesto su uso en prevención primaria para pacientes seleccionados (6) (Ver Recado ASA en prevención cardiovascular primaria).
Aunque no se conoce con exactitud el mecanismo por el cual reduce la incidencia de diferentes tipos de cáncer, se ha propuesto que la inhibición de la COX desencadena un aumento en la apoptosis y una disminución en la producción de prostaglandinas (moléculas que aumentan la producción de sustancias proinflamatorias). También se postula un mecanismo independiente de la COX que no se ha descrito con precisión (7). Sin embargo, el uso prolongado de ASA se asocia con sangrados potencialmente graves a nivel gastrointestinal (8) e intracraneal (9,10).
Recientemente, la guía australiana de cáncer colorrectal (11) introdujo el uso de ASA como herramienta de prevención en pacientes entre 50-70 años, con un tiempo de tratamiento de al menos 2.5 años, siempre que la expectativa de vida sea >10 años y no existan contraindicaciones para su uso. Para aclarar la relación riesgo/beneficio de esta intervención se encuentra en curso un ensayo clínico aleatorizado doble ciego (clinicaltrials.gov, ASPIRED NCT02394769).
Por lo anterior, el objetivo del presente Recado es evaluar el impacto del uso de ASA como estrategia de prevención primaria para cáncer colorrectal, reseñando la revisión sistemática y metaanálisis producida por el Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF, por sus siglas en inglés) de septiembre de 2021 (12). Este estudio fue seleccionado por su rigor metodológico y la vigencia de sus resultados.
Información en la que se basa este Recado
Esta revisión sistemática con metaanálisis (Síntesis de evidencia No 211 del USPSTF) es una actualización de las recomendaciones formuladas en 2016 sobre ASA (prevención de eventos cerebrovasculares, CCR y efectos adversos) que incluye un modelo de decisión basado en simulación. Para este Recado se extrajeron los datos de eficacia (incidencia y mortalidad) y seguridad (sangrado gastrointestinal, hemorragia intracraneal, accidente cerebrovascular [ACV] y sangrado mayor) del tratamiento con ASA en prevención primaria de CCR provenientes de ensayos controlados aleatorizados (ECA), estudios observacionales y de cohortes.
Resultados
La tabla 1 resume los resultados de eficacia y seguridad con el uso de ASA para esta indicación:
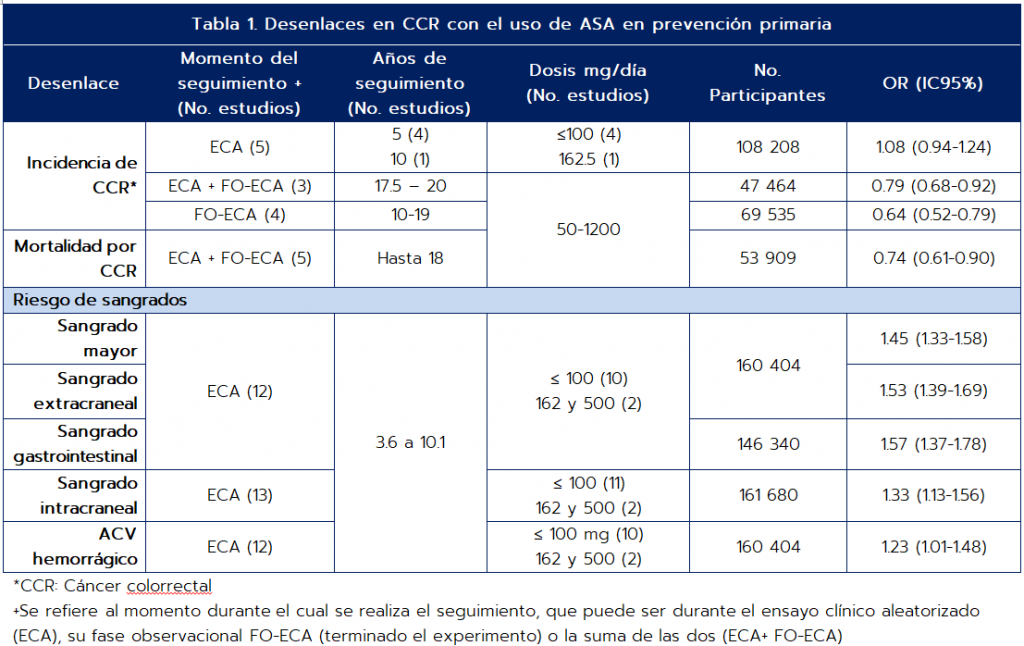
Otros resultados de interés:
Con relación a la incidencia de CCR:
En el análisis por subgrupos, 2 estudios mostraron que la reducción en la incidencia de CCR se da en los grupos más jóvenes:
- Estudio WHS (13): HR 0.71, IC95% 0.52-0.98 a 26 años de seguimiento en pacientes de 45-54 años.
- Estudio JPAD (14): HR 0.41, IC95% 0.15-0.97 a 10.7 años en el grupo <65 años.
- No se encontraron diferencias por sexo, raza, etnia o antecedente de diabetes mellitus. El estudio WHS (13) aportó el 84% de la población incluida en esta revisión, incluyó solo mujeres y solo usó dosis baja de ASA (<100mg/día).
Con relación al riesgo de sangrados:
El análisis por subgrupos muestra que no hay diferencia por dosis para sangrado gastrointestinal. En el grupo que recibió <100 mg/día de ASA, la ocurrencia de ACV hemorrágico no alcanzó significancia estadística. No hubo diferencia por edad, sexo, raza, etnia, antecedente de diabetes o categoría de riesgo cardiovascular.
Información sobre la evidencia que soporta este Recado
La calidad de la revisión sistemática es alta según la herramienta AMSTAR 2. Los autores de la revisión concluyen que la confianza en la evidencia es muy baja debido a:
- Tiempo de seguimiento de aproximadamente 5 años en la mayoría de ECA, insuficiente para evaluar incidencia de CCR.
- El tiempo de seguimiento posensayo tuvo un diseño observacional con pérdida de la aleatorización, reducción de la adherencia y el seguimiento de pacientes.
- Gran imprecisión en las estimaciones por el bajo número de casos.
De acuerdo con la metodología GRADE, la certeza en la evidencia es muy baja para incidencia y mortalidad y baja para los desenlaces de seguridad (Ver tabla GRADE).
Referencias
Cuenta de Alto Costo. 2022. Día internacional del cáncer de colon | Cuenta de Alto Costo. [online] Disponible es: http://bitly.ws/sNXc
Gco.iarc.fr. 2022. Cancer today. [online] Disponible en: http://bitly.ws/sNX4
Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, Bray F. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. 2021 May;71(3):209-249. doi: 10.3322/caac.21660. Epub 2021 Feb 4. PMID: 33538338. Disponible en: https://pubmed.ncbi.nlm.nih.gov/33538338/
Vane JR, Botting RM. The mechanism of action of aspirin. Thromb Res. 2003 Jun 15;110(5-6):255-8. doi: 10.1016/s0049-3848(03)00379-7. PMID: 14592543. Disponible en: https://pubmed.ncbi.nlm.nih.gov/14592543/
Nemerovski CW, Salinitri FD, Morbitzer KA, et al. Aspirin for primary prevention of cardiovascular disease events. Pharmacotherapy. 2012;32(11):1020-35. PMID: 23019080. Disponible en: https://pubmed.ncbi.nlm.nih.gov/23019080/
Gdovinova Z, Kremer C, Lorenzano S, Dawson J, Lal A, Caso V. Aspirin for Primary Stroke Prevention; Evidence for a Differential Effect in Men and Women. Front Neurol. 2022 Jun 21;13:856239. doi: 10.3389/fneur.2022.856239. PMID: 35800088; PMCID: PMC9254866. Disponible en: https://www.frontiersin.org/articles/10.3389/fneur.2022.856239/full
Garcia-Albeniz X, Chan AT. Aspirin for the prevention of colorectal cancer. Best Pract Res Clin Gastroenterol. 2011;25(4-5):461-72. PMID: 22122763. Disponible en: https://pubmed.ncbi.nlm.nih.gov/22122763/
Wallace JL. Prostaglandins, NSAIDs, and gastric mucosal protection: why doesn't the stomach digest itself? Physiological reviews. 2008;88(4):1547-65. PMID: 18923189. Disponible en: https://pubmed.ncbi.nlm.nih.gov/18923189/
Ascend Study Collaborative Group, Bowman L, Mafham M, et al. Effects of Aspirin for Primary Prevention in Persons with Diabetes Mellitus. N Engl J Med. 2018;379(16):1529-39. PMID: 30146931. Disponible en: http://bitly.ws/sNZa
Huang W, Saver JL, Wu Y, Lin C, Lee M, Ovbiagele B. Frequency of Intracranial Hemorrhage With Low-Dose Aspirin in Individuals Without Symptomatic Cardiovascular Disease: A Systematic Review and Meta-analysis. JAMA Neurol. 2019;76(8):906–914. doi:10.1001/jamaneurol.2019.1120 Disponible en: http://bitly.ws/sNZc
Cancer Council Australia Colorectal Cancer Guidelines Working Party. Clinical practice guidelines for the prevention, early detection and management of colorectal cancer. Sydney: Cancer Council Australia. http://bitly.ws/sNZ9
Guirguis-Blake JM, Evans CV, Perdue LA, Bean SI, Senger CA. Aspirin Use to Prevent Cardiovascular Disease and Colorectal Cancer: An Evidence Update for the U.S. Preventive Services Task Force. Evidence Synthesis No. 211. Rockville, MD: Agency for Healthcare Research and Quality; 2021. AHRQ publication no. 21-05283-EF-1. Disponible en: http://bitly.ws/sNZe
Steering Committee of the Physicians' Health Study Research Group. Final report on the aspirin component of the ongoing Physicians' Health Study. N Engl J Med. 1989 Jul 20;321(3):129-35. doi: 10.1056/NEJM198907203210301. PMID: 2664509. Disponible en: https://pubmed.ncbi.nlm.nih.gov/2664509/