Versión 4 - 25/05/22
Resultados de ensayos clínicos indican que en pacientes con COVID-19 leve el uso de ivermectina no tiene efecto favorable. Por tanto, no se recomienda como tratamiento para reducir la progresión clínica de pacientes con infección por SARS-CoV-2.
Certeza de la evidencia: moderada (por imprecisión en los resultados de los ECA incluidos)
Buena práctica para pacientes
• Se recomienda tener precaución con fuentes de información no oficiales que respalden o promuevan el uso del medicamento.
• No se deben tomar preparaciones del medicamento para uso externo (sobre la piel) o uso veterinario.
Otros mensaje clave:
- El uso excesivo o indebido de ivermectina incrementa el riesgo de efectos adversos y sobredosis (1).
- Se han reportado diversos efectos* por sobredosis de ivermectina incluyendo gastrointestinales** y neurológicos***. También puede potenciar el efecto de agentes depresores del sistema nervioso central (benzodiacepinas y barbitúricos) (1).
- Se encuentran aún en curso numerosos estudios de evaluación de ivermectina para tratamiento o prevención de COVID-19 (2).
*Dolor de cabeza, visión borrosa, mareos, taquicardia, se asocia con hipotensión.
**Náusea, vómito, dolor abdominal, diarrea.
***Disminución de conciencia, confusión, alucinaciones, pérdida de coordinación y equilibrio, convulsiones, coma y muerte.
Es importante saber lo que no se conoce
Con la evidencia actual no hay certeza de la eficacia de la ivermectina para prevenir la infección por SARS-CoV-2 (quimioprofilaxis).
Antecedentes
Con base en estudios in vitro, la ivermectina se consideró como posible opción terapéutica para COVID-19. Sin embargo, estos resultados se observaron a concentraciones muy superiores a las asociadas con las dosis recomendadas clínicamente (3,4,5) como antiparasitario en diversas enfermedades tropicales. En las condiciones usuales la ivermectina presenta un buen perfil de seguridad (6).
Siguiendo estos hallazgos se publicaron numerosos estudios evaluando el potencial de la ivermectina en la profilaxis de la infección por SARS-CoV-2 y el tratamiento de la COVID-19, así como revisiones sistemáticas y metaanálisis. De estos estudios, producidos en relativamente corto tiempo, algunos fueron de pobre calidad metodológica (7,8) y otros retractados ante diversos cuestionamientos (9,10,11). Con la información disponible para el momento, se publicó un Recado en marzo del 2021 que incluyo en su análisis el Ensayo Clínico Aleatorizado (ECA) de Elgazzar et al. (12), que fue luego retirado por posible información fraudulenta.
En el contexto de la pandemia, la ivermectina ha representado un caso único de alta demanda del público y los sistemas de salud por información, y una oferta con escaso rigor. La posterior retractación de algunos estudios ha generado controversia sobre la conducta ética en investigación en una emergencia sanitaria, dada la duración de los procesos entre la generación y el uso de conocimiento (15). En Latinoamérica, la ivermectina se autorizó inicialmente en algunos países e incluso fue recomendada en las guías de práctica clínica de Bolivia y Perú (16,17). Actualmente la OMS recomienda se use solamente como agente experimental en el contexto de ECA de COVID-19 (18).
Este Recado presenta una actualización de la evidencia disponible sobre el uso de ivermectina para la prevención de complicaciones en pacientes con infección por SARS-CoV-2.
Información en la que se basa este Recado
Se realizó búsqueda en PubMed, en la cual se encontraron 28 revisiones sistemáticas y 18 ECA (ver estrategia). Se seleccionaron para esta actualización los estudios de Reis et al (19), Chaccour et al (20), Vallejos et al (21), que son ensayos clínicos controlados, aleatorizados, comparados con placebo y realizados en pacientes ambulatorios, que agregan nueva evidencia al estudio de López-Medina et al (22).
Para esta versión se excluyeron los ECA de Niaee et al. (23) y Elgazzar et al. (12), dado que el primero compara con una intervención sin eficacia comprobada para tratamiento de COVID-19 (hidroxicloroquina 200mg dos veces/día) y presenta alto riesgo de sesgo. El segundo, porque fue retirado por posible fraude. Ambos estudios, que incluían pacientes hospitalizados, favorecían el uso de ivermectina.
Resultados
Los cuatro ECA incluidos reclutaron pacientes durante 1 a 6 meses, en Brasil (19), España (20), Argentina (21) y Colombia (22), incluyendo 12-679 participantes por grupo, con mediana de edad 26-49 años. Se suministró ivermectina por vía oral en dosis de 192.4 mcg/kg/día durante 2 días (21) – 427 mcg/kg dosis única (20). El período de seguimiento varió entre 21 (22) y 30 días (21). La información de cada ECA se encuentra en detalle en la tabla 1.
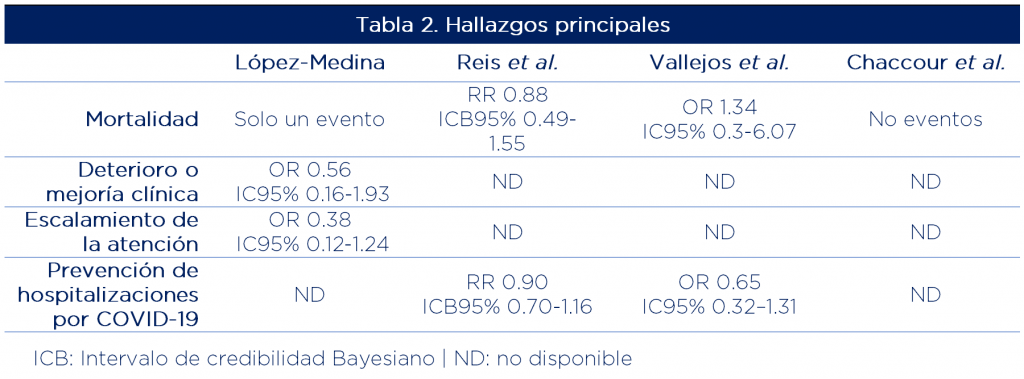
Los hallazgos principales de los ECA incluidos fueron (ver tabla 2):
- No se identificaron diferencias en los desenlaces clínicos evaluados: mortalidad, deterioro clínico, escalamiento de la atención y resolución completa de síntomas.
- La proporción de pacientes PCR SARS-CoV-2 positivos a los 7 días de tratamiento fue similar entre los grupos en un estudio (20).
- En cuanto a tolerancia, un ECA (22) reporto suspensión del tratamiento por eventos adversos en 7.5% (n=15) de los participantes del grupo de ivermectina y 2.5% (n=5) del grupo control y eventos serios en 4 participantes (2 c/grupo).
Información sobre la evidencia que soporta este Recado
Según el instrumento RoB2 (24) los estudios de Reis et al (19), Chaccour et al (20) y Vallejos et al (21), se califican con bajo riesgo de sesgo. El estudio de López-Medina et al se calificó como riesgo de sesgo no evaluable por presentar problemas en su conducción al no cumplir el protocolo original.
La calidad de la evidencia se consideraría moderada para prevenir hospitalizaciones y mortalidad por imprecisión de los resultados (bajo número de eventos).
Referencias
CDC Health Alert Network. Rapid Increase in Ivermectin Prescriptions and Reports of Severe Illness Associatd with Use of Products Containing Ivermectin to Prevent or Treat COVID-19. Emergency Preparedness and Response. Centers for Disease Control and Prevention. Available from: https://emergency.cdc.gov/han/2021/han00449.asp.
S. National Library of Medicine. Clinical trials. Ivermectin/ COVID-19 – SARS-CoV-2. Consultado el 22 de febrero de 2022. Available from: Search of: ivermectin | Recruiting, Not yet recruiting Studies | COVID-19 - List Results - ClinicalTrials.gov
Pan American Health O. Ongoing Living Update of Potential COVID-19 Therapeutics: summary of rapid systematic reviews. 2020;17. Available from: https://iris.paho.org/handle/10665.2/52719
Heidary F, Gharebaghi R. Ivermectin: a systematic review from antiviral effects to COVID-19 complementary regimen. J Antibiot (Tokyo) [Internet]. 2020;(December 2019). Available from: http://dx.doi.org/10.1038/s41429-020-0336-z
Caly L, Druce JD, Catton MG, Jans DA, Wagstaff KM. The FDA-approved drug ivermectin inhibits the replication of SARS-CoV-2 in vitro. Antiviral Res. 2020;178(March):3–6.
Navarro M, Camprubí D, Requena-Méndez A, Buonfrate D, Giorli G, Kamgno J, Gardon J, Boussinesq M, Muñoz J, Krolewiecki A. Safety of high-dose ivermectin: a systematic review and meta-analysis. J Antimicrob Chemother. 2020 Apr 1;75(4):827-834. doi: 10.1093/jac/dkz524. PMID: 31960060.
Rothrock, Steven G. MD; Weber, Kurt D. MD; Giordano, Philip A. MD; Barneck, Mitchell D. MD. Meta-Analyses Do Not Establish Improved Mortality With Ivermectin Use in COVID-19, American Journal of Therapeutics: January/February 2022 - Volume 29 - Issue 1 - p e87-e94 doi: 10.1097/MJT.0000000000001461
Lawrence JM, Meyerowitz-Katz G, Heathers JAJ, Brown NJL, Sheldrick KA. The lesson of ivermectin: meta-analyses based on summary data alone are inherently unreliable. Nat Med. 2021 Nov;27(11):1853-1854. doi: 10.1038/s41591-021-01535-y. PMID: 34552263.
Hill, A., Garratt, A., Levi, J., Falconer, J., Ellis, L., McCann, K., Pilkington, V., Qavi, A., Wang, J., & Wentzel, H. (2022). Retraction to: Meta-analysis of Randomized Trials of Ivermectin to Treat SARS-CoV-2 Infection. Open forum infectious diseases, 9(3), ofac056. https://doi.org/10.1093/ofid/ofac056
Samaha AA, Mouawia H, Fawaz M, Hassan H, Salami A, Bazzal AA, Saab HB, Al-Wakeel M, Alsaabi A, Chouman M, Moussawi MA, Ayoub H, Raad A, Hajjeh O, Eid AH, Raad H. Retraction: Samaha et al. Effects of a Single Dose of Ivermectin on Viral and Clinical Outcomes in Asymptomatic SARS-CoV-2 Infected Subjects: A Pilot Clinical Trial in Lebanon. Viruses 2021,13, 989. Viruses. 2021 Oct 26;13(11):2154. doi: 10.3390/v13112154. PMID: 34751680; PMCID: PMC8577689.
Zaidi AK, Dehgani-Mobaraki P. RETRACTED ARTICLE: The mechanisms of action of Ivermectin against SARS-CoV-2: An evidence-based clinical review article. J Antibiot (Tokyo). 2022 Feb;75(2):122. doi: 10.1038/s41429-021-00430-5. Epub 2021 Jun 15. PMID: 34127807; PMCID: PMC8203399.
Elgazzar A, Hany B, Youssef SA, Hafez M. Efficacy and Safety of Ivermectin for Treatment and prophylaxis of COVID-19 Pandemic. medRxiv [Internet]. 2020;1–13. Available from: https://www.researchsquare.com/article/rs-100956/v1
Popp M, Stegemann M, Metzendorf MI, Gould S, Kranke P, Meybohm P, Skoetz N, Weibel S. Ivermectin for preventing and treating COVID-19. Cochrane Database Syst Rev. 2021 Jul 28;7(7):CD015017. doi: 10.1002/14651858.CD015017.pub2. PMID: 34318930; PMCID: PMC8406455.
Lim SCL, Hor CP, Tay KH, et al. Efficacy of Ivermectin Treatment on Disease Progression Among Adults with Mild to Moderate COVID-19 and Comorbidities: The I-TECH Randomized Clinical Trial. JAMA Intern Med. Published online February 18, 2022. doi:10.1001/jamainternmed.2022.0189
El-Menyar A, Mekkodathil A, Asim M, Consunji R, Rizoli S, Abdel-Aziz Bahey A, Al-Thani H. Publications and retracted articles of COVID-19 pharmacotherapy-related research: A systematic review. Sci Prog. 2021 Apr-Jun;104(2):368504211016936. doi: 10.1177/00368504211016936. PMID: 33989091
Ministerio de Salud y Deporte de Bolivia (2020) Ministerio de salud autoriza uso de ivermectina contra el COVID-19 bajo protocolo.12 de mayo 2020. Disponible en: www.minsalud.gob.bo/4157-ministerio-de-salud-autoriza-uso-de-ivermectina-contra-el-covid-19-bajo-protocolo.
Ministerio de salud (2020) RM375.Documento técnico: Manejo ambulatorio de personas afectadas por COVID-19 en el Perú. Junio 2020.
World Health Organization (2022). Therapeutics and COVID-19. Living guideline. Published on 1/13/22. Available from: https://www.who.int/publications/i/item/WHO-2019-nCoV-therapeutics-2022.1
Reis G, Silva EASM, Silva DCM, Thabane L, Milagres AC, Ferreira TS, Dos Santos CVQ, Campos VHS, Nogueira AMR, de Almeida APFG, Callegari ED, Neto ADF, Savassi LCM, Simplicio MIC, Ribeiro LB, Oliveira R, Harari O, Forrest JI, Ruton H, Sprague S, McKay P, Guo CM, Rowland-Yeo K, Guyatt GH, Boulware DR, Rayner CR, Mills EJ; TOGETHER Investigators. Effect of Early Treatment with Ivermectin among Patients with Covid-19. N Engl J Med. 2022 Mar 30. doi: 10.1056/NEJMoa2115869. Epub ahead of print. PMID: 35353979.
Chaccour, C., Casellas, A., Blanco-Di Matteo, A., Pineda, I., Fernandez-Montero, A., Ruiz-Castillo, P., Richardson, M. A., Rodríguez-Mateos, M., Jordán-Iborra, C., Brew, J., Carmona-Torre, F., Giráldez, M., Laso, E., Gabaldón-Figueira, J. C., Dobaño, C., Moncunill, G., Yuste, J. R., Del Pozo, J. L., Rabinovich, N. R., Schöning, V., … Fernández-Alonso, M. (2021). The effect of early treatment with ivermectin on viral load, symptoms and humoral response in patients with non-severe COVID-19: A pilot, double-blind, placebo-controlled, randomized clinical trial. EClinicalMedicine, 32, 100720. https://doi.org/10.1016/j.eclinm.2020.100720
Vallejos J, Zoni R, Bangher M, Villamandos S, Bobadilla A, Plano F, Campias C, Chaparro Campias E, Medina MF, Achinelli F, Guglielmone HA, Ojeda J, Farizano Salazar D, Andino G, Kawerin P, Dellamea S, Aquino AC, Flores V, Martemucci CN, Martinez SM, Segovia JE, Reynoso PI, Sosa NC, Robledo ME, Guarrochena JM, Vernengo MM, Ruiz Diaz N, Meza E, Aguirre MG. Ivermectin to prevent hospitalizations in patients with COVID-19 (IVERCOR-COVID19) a randomized, double-blind, placebo-controlled trial. BMC Infect Dis. 2021 Jul 2;21(1):635. doi: 10.1186/s12879-021-06348-5. PMID: 34215210; PMCID: PMC8250562
López-Medina E, López P, Hurtado IC, et al. Effect of Ivermectin on Time to Resolution of Symptoms Among Adults With Mild COVID-19: A Randomized Clinical Trial. 2021;325(14):1426–1435. doi:10.1001/jama.2021.3071
Niaee MS, Gheibi N, Namdar P, Allami A, Zolghadr L, Javadi A, et al. Ivermectin as an adjunct treatment for hospitalized adult COVID-19 patients: A randomized multi-center clinical trial. Asian Pac J Trop Med [serial online] 2021; 14: 266-73 Available from: https://www.apjtm.org/article.asp?issn=1995-7645;year=2021;volume=14;issue=6;spage=266;epage=273;aulast=Shakhsi
Sterne J, Savović J, Page M, Elbers R, Blencowe N, Boutron I, et al. RoB 2: a revised tool for assessing risk of bias in randomised trials. BMJ. 2009;(366):l4898.