Versión 1 - 29/07/20
La tomografía axial computarizada (TAC) de tórax no se considera una prueba que pudiera sustituir a la RT-PCR en el diagnóstico inicial de la COVID-19, dada la alta tasa de hallazgos imagenológicos en pacientes con pruebas moleculares negativas. Por esta razón, las dos pruebas aportan información complementaria que, sumada a otros criterios, ayuda a establecer un diagnóstico clínico válido.
Calidad de la evidencia: baja a muy baja (estudios con riesgo de sesgo, inconsistencia en resultados e imprecisión en las estimaciones).
Otros mensajes clave:
- El uso de la TAC de tórax como prueba inicial de diagnóstico de la COVID-19, especialmente en escenarios de baja prevalencia, implicaría un alto consumo de recursos del sistema de salud sin aumentar el beneficio en la identificación de casos.
- Aun en escenarios de mayor prevalencia (>30%), la TAC de tórax por sí sola no logra sustituir a la RT-PCR en el diagnóstico de la enfermedad.
Es importante saber lo que no se conoce
No se conoce el desempeño diagnóstico de la TAC de tórax en relación con el tiempo de inicio de los síntomas de la enfermedad.
Antecedentes
Actualmente, la RT-PCR continúa siendo la principal herramienta para diagnosticar la infección por SARS-CoV-2 (1,2). Las limitaciones de esta prueba incluyen la dificultad en la recolección de la muestra, el alto consumo de suministros y de tiempo para la obtención de resultados y su relación con el tiempo de aparición de los síntomas. Estos factores aumentan la probabilidad de falsos negativos, generando problemas en la clasificación oportuna y adecuada de los casos y, por tanto, la necesidad de buscar otras herramientas diagnósticas (3,4).
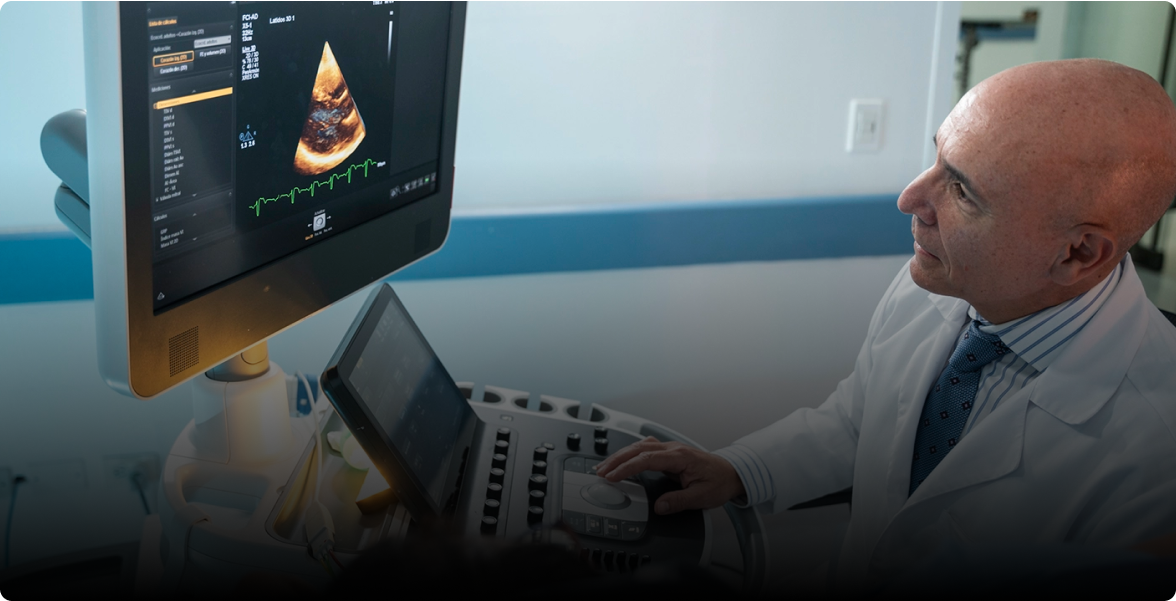
La TAC de tórax se ha propuesto como una herramienta alternativa para el diagnóstico inicial de la COVID-19 en áreas con alta prevalencia (5,6). Los hallazgos característicos de la infección por SARS-CoV-2 incluyen opacidad en vidrio esmerilado o cambios intersticiales con una distribución periférica. Estos se han observado consistentemente tanto en pacientes con prueba RT–PCR positiva como en aquellos con prueba negativa pero sintomatología sugestiva de infección por SARS-CoV-2 (7,8). Sin embargo, problemas de la TAC como la superposición de los hallazgos imagenológicos de la infección por SARS-CoV-2 con los de otras infecciones virales, así como aspectos técnicos en su realización, han limitado su utilidad para hacer este diagnóstico (9).
Este Recado reseña una revisión sistemática (10) que evalúa el rendimiento de la TAC de tórax y la RT-PCR en el diagnóstico de la COVID-19.
Información en la que se basa este Recado
La búsqueda se realizó en la Plataforma L.OVE (Living Overview of Evidence) de la Fundación Epistemonikos. Se consultó el L.OVE de Coronavirus Disease (COVID-19) que se estima, compila todos los artículos publicados a la fecha sobre esta enfermedad (disponible en: https://bit.ly/36h60fv); la pregunta en formato PICO para la búsqueda se construyó a partir de los términos COVID-19, diagnostic, imaging test y computed tomography (11).
Se identificaron nueve revisiones sistemáticas (RS) y 141 estudios primarios incluyendo estudios en curso y protocolos registrados, de los cuales solo una RS reportaba resultados que respondían a la pregunta PICO de interés (10).
Hallazgos
Kim et al. adelantaron una RS de la literatura con el objetivo de evaluar el rendimiento diagnóstico de la TAC de tórax en relación con la RT-PCR para diagnosticar COVID-19 clínicamente relevante. Los autores realizaron la búsqueda desde diciembre 1 de 2019 hasta abril 3 de 2020 dirigida a estudios que reportaran sensibilidad y especificidad. El estándar de referencia fue el resultado de la prueba de RT-PCR por su alta especificidad (99% en segunda prueba).
La RS incluyó 68 estudios que cumplían con los criterios de inclusión, de los cuales 63 (n=6218) evaluaron la TAC de tórax en pacientes de ambos sexos entre los 3 y 70 años. Solamente seis estudios reportaron tanto la sensibilidad como la especificidad.
Los estudios primarios no reportaron el momento de toma de las pruebas con respecto al inicio de los síntomas de la enfermedad. Los estimados agregados de sensibilidad y especificidad se calcularon utilizando modelos de efectos aleatorios. Se estimaron valores predictivos positivos (VPP) y predictivos negativos (VPN) asumiendo distintas tasas de prevalencia de COVID-19.
Mediante metarregresión los autores exploraron diversos factores de confusión como lugar de realización del estudio, proporción de pacientes adultos mayores, distribución de gravedad de la enfermedad, proporción de pacientes con comorbilidades, proporción de pacientes asintomáticos y uso de genes ORF (open reading frame por sus siglas en inglés) en las pruebas RT-PCR.
Los principales hallazgos fueron:
- La estimación agregada de sensibilidad de la TAC de tórax basada en el total de estudios fue 94% (IC95% 91-96%) (63 estudios, n=6218, I2= 95%).
- La estimación agregada de especificidad de la TAC de tórax basada en el total de estudios fue 37% (IC95% 26-50%)(5 estudios, n=620, I2= 83%).
- La estimación de sensibilidad agregada de la TAC de tórax (tomando como estándar RT-PCR positiva en dos o más pruebas) fue 93% (IC95% 88-96%)(21 estudios, n=1564, I2= 87%) y la especificidad agregada fue 35% (IC95% 23-48%) (4 estudios, n=605, I2= 86%).
- La proporción de pacientes con hallazgos en la TAC y resultados negativos de RT-PCR (“falsos positivos” teniendo la prueba como referencia) resulta considerablemente alta (455/1000).
- Los resultados de los estudios incluidos mostraron importante heterogeneidad (I2 entre 80% y 95%).
Información sobre la evidencia que soporta este Recado:
La revisión de Kim et al. evaluó la calidad de los estudios incluídos con la herramienta QUADAS-2 (12). Los autores calificaron los estudios en general como de riesgo de sesgo bajo en aspectos como selección de pacientes y el momento de realización de las pruebas diagnóstica y de referencia; y como riesgo de sesgo no claro en aspectos relacionados con los procedimientos de la RT-PCR como prueba de referencia. El sesgo de publicación lo evaluaron como bajo.
La RS fue calificada como de riesgo de sesgo moderado. De acuerdo con la aproximación GRADE, los estudios incluidos tenían riesgo de sesgo serio, inconsistencia seria e imprecisión seria en las estimaciones. La evidencia fue calificada como baja para sensibilidad y muy baja para especificidad.
Referencias
Grassly NC, Pons-salort M, Parker EPK, White PJ, Ainslie K, Baguelin M. Report 16: Role of testing in COVID-19 control. 2020.
Universidad de Antioquia. Desempeño clínico de las pruebas diagnósticas de laboratorio en la infección por SARS-CoV-2 Respuesta de 10 días. 2020.
Xie X, Zhong Z, Zhao W, Zheng C, Wang F, Liu J. Chest CT for Typical 2019-nCoV Pneumonia: Relationship to Negative RT-PCR Testing. Radiology. 2020;200343.
Ai T, Yang Z, Hou H, Zhan C, Chen C, Lv W, et al. Correlation of Chest CT and RT-PCR Testing in Coronavirus Disease 2019 (COVID-19) in China: A Report of 1014 Cases. Radiology. 2020;2019:200642.
Bachelet VC. ¿Conocemos las propiedades diagnósticas de las pruebas usadas en COVID-19? Una revisión rápida de la literatura recientemente publicada. Medwave. 2020;20(3):e7890.
Kim H, Hong H, Yoon SH. Diagnostic Performance of CT and Reverse Transcriptase-Polymerase Chain Reaction for Coronavirus Disease 2019: A Meta-Analysis. Radiology. 2020;201343.
STR, ASER. STR/ASER COVID-19 position statement [Internet]. 2020 [cited 2020 Jul 16]. Available from: https://thoracicrad.org/
Fang Y, Zhang H, Xie J, Lin M, Ying L, Pang P, et al. Sensitivity of Chest CT for COVID-19: Comparison to RT-PCR. Radiology. 2020;
Chung M, Bernheim A, Mei X, Zhang N, Huang M, Zeng X, et al. CT imaging features of 2019 novel coronavirus (2019-NCoV). Radiology. 2020;295(1):202–7.
L.OVE platform. Diagnostic accuracy or impact of performing computed tomography for Coronavirus infection [Internet]. 2020 [cited 2020 Jul 16]. Available from: https://bit.ly/335admV
Arevalo-Rodriguez I, Buitrago-Garcia D, Simancas-Racines D, Zambrano-Achig P, Campo R del, Ciapponi A, et al. False-negative results of initial RT-PCR assays for COVID-19: a systematic review. medRxiv [Internet]. 2020;2020.04.16.20066787. Available from: http://medrxiv.org/lookup/doi/10.1101/2020.04.16.20066787
Ciapponi A. QUADAS-2 : instrumento para la evaluación de la calidad de estudios de precisión diagnóstica. Evidencia [Internet]. 2015;22–6. Available from: http://www.foroaps.org/files/64fe85009abba8c506e903adf90dbc17.pdf