Versión 1 - 31/07/2023
Evidencia observacional consistente sugiere que el consumo de endulzantes no azucarados podría tener una asociación leve a moderada con mayor riesgo de eventos cardiovasculares. Aunque estos hallazgos no han sido replicados por ensayos clínicos, que muestran un efecto neutro en desenlaces subrogados, se sugiere que además de limitar el consumo de azúcar, se evite sustituirlo con endulzantes no azucarados mientras se conoce nueva y mejor evidencia.
Certeza en la evidencia: baja a muy baja por riesgo de sesgos e imprecisión y no documentación de efecto dosis-respuesta.
Otros mensajes clave:
- La evidencia experimental no encontró beneficio de los endulzantes no azucarados para reducir cifras de presión arterial o niveles de lípidos.
- Con relación a los cambios en el peso corporal, los resultados entre los estudios observacionales y experimentales fueron contradictorios.
- En los estudios observacionales, los endulzantes no azucarados se asocian a mayor riesgo de obesidad, hipertensión arterial y diabetes.
Es importante saber lo que no se conoce:
Se desconocen los mecanismos fisiopatológicos que explican la asociación de los endulzantes no azucarados con mayor riesgo de eventos cardiovasculares.
Antecedentes
Los carbohidratos son esenciales en la alimentación humana como sustrato energético y para la construcción de macromoléculas (1). En la dieta se consumen en diferentes formas, incluyendo azúcares libres o añadidos (2,3). El proceso de industrialización de los últimos siglos ha llevado, entre otras, a aumento del consumo calórico debido en parte a la oferta de alimentos procesados. Entre estos se destacan las bebidas endulzadas con azúcar (BEA*), las cuales han sido el principal referente para la medición del consumo de azúcares en la población general (4).
*Cualquier bebida que contenga edulcorantes calóricos agregados como sacarosa, jarabe de maíz de alta fructosa o concentrados de jugo de frutas.
Se ha investigado el efecto metabólico del consumo de azúcares añadidos y su impacto en la salud cardiovascular. Un estudio que integra revisiones sistemáticas sobre el uso de BEA encontró aumento del riesgo para diabetes tipo 2 (27%), enfermedad coronaria (17%), síndrome metabólico (14%), obesidad (12%), hipertensión (11%), enfermedad cardiovascular (8%), muerte cardiovascular (8%) y ataque cerebrovascular (7%) (5). El riesgo se derivaría de una baja saciedad atribuible a la ingesta de estas bebidas, que induce a mayor consumo calórico, con posterior ganancia de peso (6). Sin embargo, la certeza en la evidencia de estos hallazgos ha sido consistentemente baja a muy baja (5).
Por lo anterior, la OMS ha recomendado que la ingesta de azúcares de la dieta no exceda el 10% del total de las calorías/día (6) y se limiten los consumos de azúcar libre o añadido y BEA a menos de 25 gr/día (<6 cucharaditas/día) y 200-355 mL/semana, respectivamente (7). Sin embargo, el consumo creciente de las BEA (4,9) ha llevado a promover políticas de impuestos para desincentivar su uso (9).
Al comparar el consumo mundial de bebidas azucaradas entre 1990 y 2015, se observa un incremento en países de América del Sur y Central y partes del sur y norte de África. En Colombia, por ejemplo, el consumo pasó de 400-499 a 500-600 gr/día (4). Las tendencias de consumo entre los jóvenes generalmente han sido paralelas a las de los adultos, destacándose que el 54% de los adolescentes consumen BEA al menos una vez al día (10).
Como alternativa a los azucares de la dieta se han introducido endulzantes no azucarados (ENA) incluyendo aspartame, neotame, sacarina, esteviol, sucralosa, entre otros. Estas sustancias tienen mayor poder endulzante relativo (por ej. hasta de 13.000 veces más con neotame) con una menor carga calórica.
Actualmente se cuenta con recomendaciones sobre el límite en el consumo de los ENA (12,13). A pesar de los beneficios en términos de ingesta calórica, la evidencia reciente también ha mostrado asociación con aumento de peso y eventos cardiovasculares (13,14). En consecuencia, la OMS ha sugerido no usar los ENA como medio para controlar el peso o reducir el riesgo de enfermedades crónicas no transmisibles (15). Esta recomendación ha sido controvertida por sustentarse en evidencia predominantemente observacional (16,17).
Por esta razón, el presente Recado aborda el efecto de los ENA en la salud cardiovascular en adultos sin diabetes.
Información en la que se basa este Recado
La estrategia de búsqueda incluyó los términos “sweetening agents”, “sugar substitutes”, “artificial sugars” y “cardiovascular disease” en las bases de datos Medline/Pubmed, Embase y Cochrane. De 235 registros recuperados, se consideraron relevantes los estudios de Toewns et al (13), Yin et al (18), Diaz et al (19) y Ríos et al (20). Se seleccionó este último por la focalización temática, rigor metodológico y vigencia.
La revisión sistemática (RS) de Ríos et al (20) incluyó estudios tanto experimentales como observacionales, realizados en adultos, niños y mujeres embarazadas predominantemente sanos. Los autores excluyeron estudios realizados exclusivamente en adultos con prediabetes, diabetes o poblaciones con otras enfermedades (excepto para estudios de casos y controles con controles de pacientes hospitalarios, que se incluyeron para el desenlace de cáncer).
Esta RS comparó el consumo de ENA con dosis más bajas/ningún consumo. Para su inclusión, los estudios debían informar una ingesta diaria aceptable según lo establecido por el Comité conjunto de la FAO/Grupo de Expertos en Aditivos Alimentarios de la OMS (Anexo 1). En el caso de los ensayos clínicos el comparador correspondió a cualquier tipo de azúcar, placebo, agua o ninguna intervención. En los estudios con intervenciones simultáneas, se validó que estas cointervenciones fueran similares y balanceadas entre los grupos experimentales.
Para efectos de este Recado se analizaron específicamente la incidencia de desenlaces metabólicos y cardiovasculares en la población adulta. Otros desenlaces de interés incluyeron los cambios en la tensión arterial y en los niveles de lípidos.
Resultados
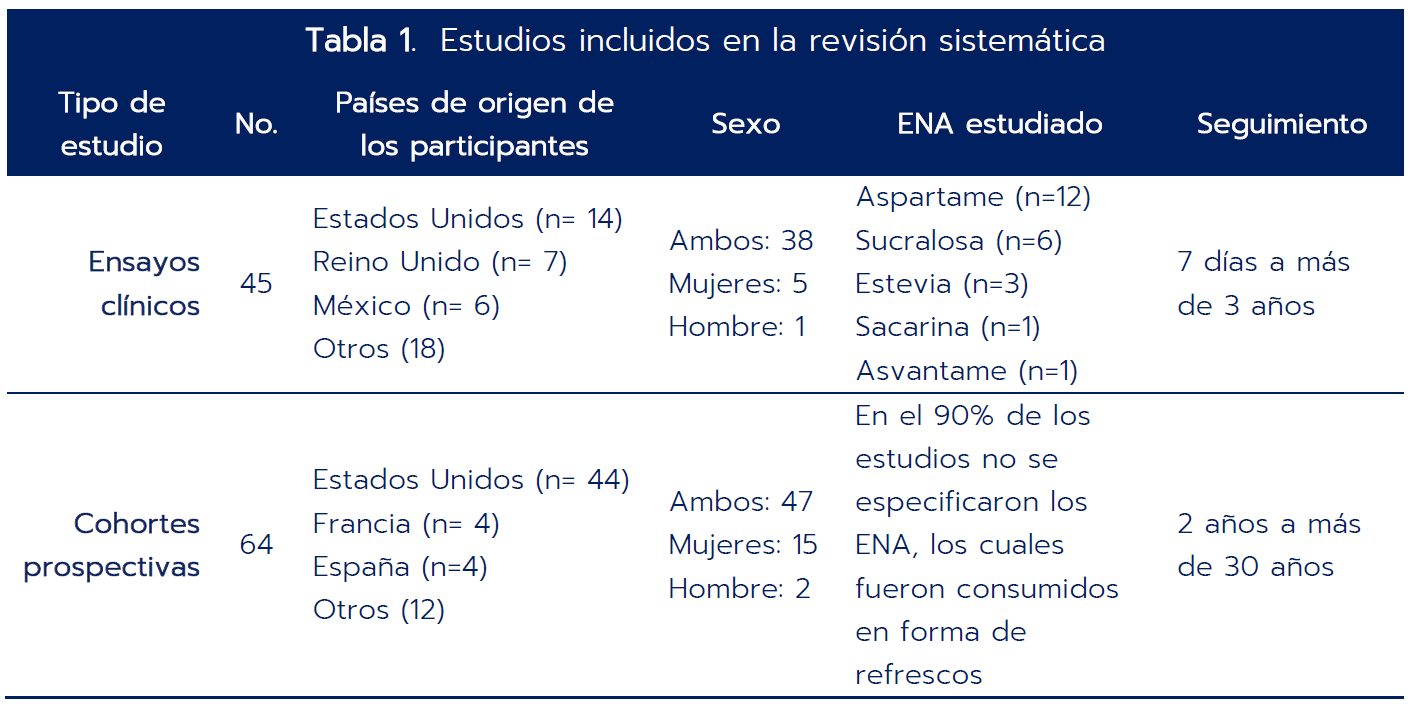
La tabla 1 resume las principales características de los estudios incluidos en la RS.
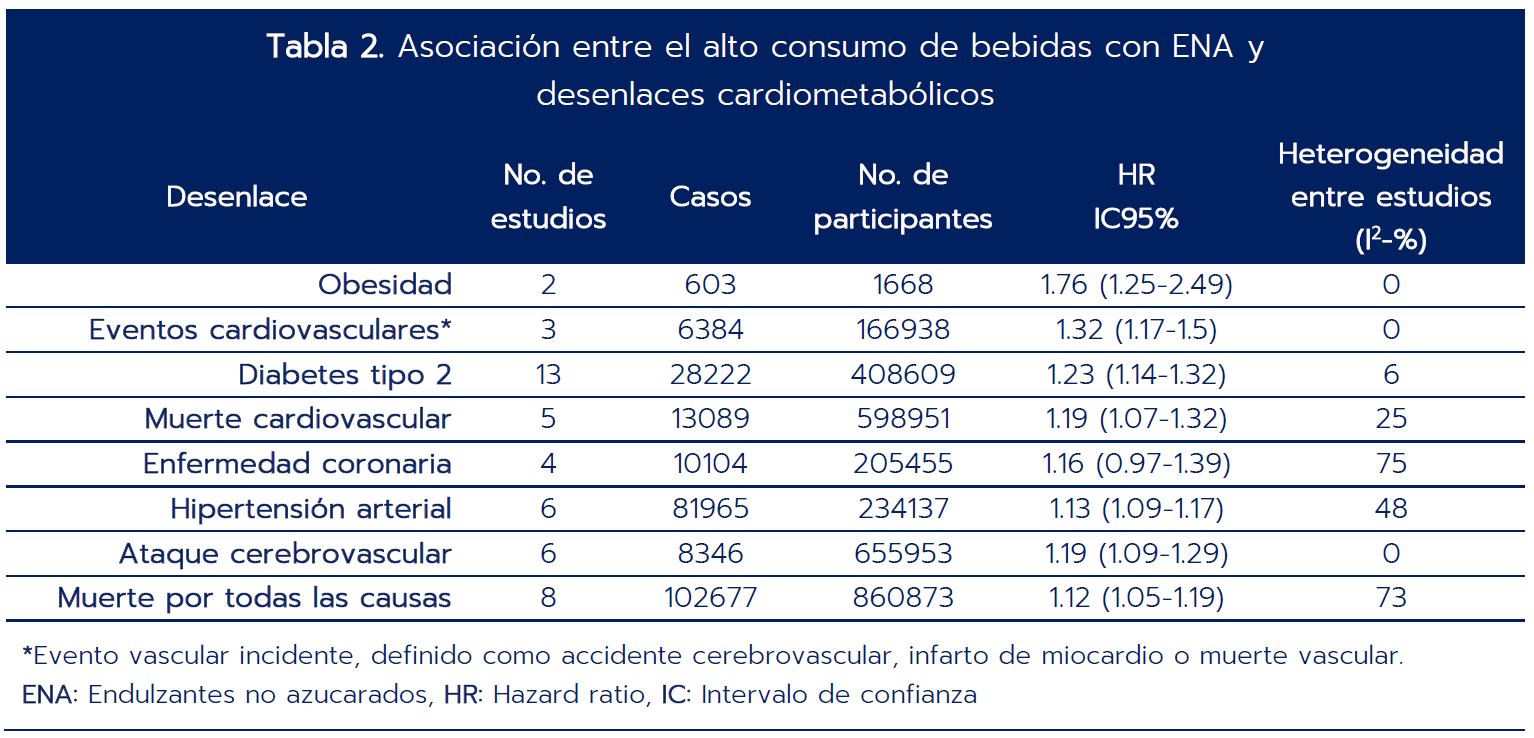
En la tabla 2 se presentan los principales resultados en eventos clínicos basados en estudios de cohorte prospectivos. Con el uso de los ENA se observó mayor riesgo de obesidad, eventos cardiovasculares, diabetes tipo 2 e hipertensión arterial.
En los ensayos clínicos se observa una disminución leve del peso corporal con ENA (MD: -0.71, IC95%: -1.13 a -0.28, I2: 83%), cuando se comparan con los azúcares de la dieta. Por el contrario, no se encontraron diferencias con relación a:
- Presión arterial sistólica (mmHg): MD: -1.33 (IC95%: -2.71 a 0.06, I2: 83%)
- Presión arterial diastólica (mmHg): MD: -0.51 (IC95%: -1.68 a 0.65, I2: 38%)
- Colesterol LDL (mg/dL): MD: 16 (IC95%: -1.16 a 3.48, I2: 32%)
- Colesterol HDL (mg/dL): MD: 0 (IC95%: -1.16 a 1.16, I2: 45%)
- Triglicéridos (mg/dL): MD: -3.5 (IC95%: -9.63 a 3.54, I2: 55%).
MD: Media de la diferencia.
Información sobre la evidencia que soporta este Recado
La aplicación de la herramienta AMSTAR 2 (21) permitió concluir confianza alta en la RS. Los autores aplicaron la herramienta ROB de Cochrane para ensayos clínicos concluyendo alto riesgo de sesgo (fallas en varios dominios). Para los de cohorte prospectiva utilizaron la escala de Newcastle–Ottawa concluyendo bajo riesgo. Sin embargo, en la reevaluación del cuerpo de evidencia observacional para este Recado se calificó como alto riesgo de sesgo (por confusión residual causalidad inversa).
La certeza global en la evidencia para los desenlaces de interés, a partir de la metodología GRADE (22), se consideró baja a muy baja (Anexo 2. tablas GRADE 1 y 2), principalmente por riesgo de sesgos e imprecisión:
- Ensayos clínicos: Baja a muy baja por riesgo de sesgos e imprecisión.
- Estudios prospectivos: Muy baja por riesgo de sesgo residual, causalidad inversa e imprecisión.
Unidad de Síntesis y Transferencia de Conocimiento | Correspondencia: jvillarc@lacardio.org
Rodríguez, J*; Villar J**; Moreno, K**; Cruz, J**; Balcázar M**+
(*)Desarrollo, (**)Edición, (+)Diseminación
¿Tienes una pregunta clínica que nuestra Unidad de Síntesis y Transferencia del Conocimiento pueda resolver a través de evidencia científica?
Sí, enviar pregunta
Referencias
Candy DJ. Biological Functions of Carbohydrates [Internet]. Dordrecht: Springer Netherlands; 1980 [consultado el 2 de julio de 2023]. Disponible en: https://doi.org/10.1007/978-94-009-8686-2
Te Morenga L, Mallard S, Mann J. Dietary sugars and body weight: systematic review and meta-analyses of randomised controlled trials and cohort studies. BMJ 2012;346:e7492. doi:10.1136/bmj.e7492
Phillips JA. Dietary Guidelines for Americans, 2020-2025. Workplace Health Saf 2021;69:395. doi:10.1177/21650799211026980
Malik VS, Hu FB. The role of sugar-sweetened beverages in the global epidemics of obesity and chronic diseases. Nat Rev Endocrinol. 2022 Apr;18(4):205-218. doi: 10.1038/s41574-021-00627-6
Huang Y, Chen Z, Chen B, Li J, Yuan X, Li J et al. Dietary sugar consumption and health: umbrella review. BMJ. 2023 Apr 5;381:e071609. doi: 10.1136/bmj-2022-071609
Malik VS, Hu FB. The role of sugar-sweetened beverages in the global epidemics of obesity and chronic diseases. Nat Rev Endocrinol. 2022 Apr;18(4):205-218. doi: 10.1038/s41574-021-00627-6
World Health Organization. Guideline: Sugars Intake for Adults and Children. World Health Organization, 2015
Ooi JY, Wolfenden L, Sutherland R, Nathan N, Oldmeadow C, Mclaughlin M, Barnes C, Hall A, Vanderlee L, Yoong SL. A Systematic Review of the Recent Consumption Levels of Sugar-Sweetened Beverages in Children and Adolescents From the World Health Organization Regions With High Dietary-Related Burden of Disease. Asia Pac J Public Health. 2022 Jan;34(1):11-24. doi: 10.1177/10105395211014642
WHO manual on sugar-sweetened beverage taxation policies to promote healthy diets. Geneva: World Health Organization; 2022. Licence: CC BY-NC-SA 3.0 IGO
Yang L, Bovet P, Liu Y, Zhao M, Ma C, Liang Y, Xi B. Consumption of Carbonated Soft Drinks Among Young Adolescents Aged 12 to 15 Years in 53 Low- and Middle-Income Countries. Am J Public Health. 2017 Jul;107(7):1095-1100. doi: 10.2105/AJPH.2017.303762.
World Cancer Research Fund International. Diet, nutrition, physical activity and cancer: A global perspective. A summary of the Third Expert Report. 2018. https://www.wcrf.org/dietandcancer/asummary-of-the-third-expert-report/
World Health Organization. Evaluations of the Joint FAO/WHO Expert Committee on Food Additives (JECFA). 2017. http://apps.who.int/food-additives-contaminants-jecfa-database/search.aspx. [PubMed]
Toews I, Lohner S, Küllenberg de Gaudry D, Sommer H, Meerpohl JJ. Association between intake of non-sugar sweeteners and health outcomes: systematic review and meta-analyses of randomised and non-randomised controlled trials and observational studies. BMJ. 2019 Jan 2;364:k4718. doi: 10.1136/bmj.k4718
Debras C, Chazelas E, Sellem L, Porcher R, Druesne-Pecollo N, Esseddik Y, de Edelenyi FS, Agaësse C, De Sa A, Lutchia R, Fezeu LK, Julia C, Kesse-Guyot E, Allès B, Galan P, Hercberg S, Deschasaux-Tanguy M, Huybrechts I, Srour B, Touvier M. Artificial sweeteners and risk of cardiovascular diseases: results from the prospective NutriNet-Santé cohort. BMJ. 2022 Sep 7;378:e071204. doi: 10.1136/bmj-2022-071204.
Use of non-sugar sweeteners: WHO guideline. Geneva: World Health Organization; 2023. Licence: CC BY-NC-SA 3.0 IGO. Disponible en: https://www.who.int/publications/i/item/9789240073616
International Sweeteners Association [Internet]. ISA scientific response to the World Health Organization (WHO) guideline on use of non-sugar sweeteners - International Sweeteners Association; [consultado el 3 de julio de 2023]. Disponible en: https://bit.ly/4bohGye
Science Media Centre [Internet]. Expert reaction to new WHO guideline which advises not to use non-sugar sweeteners for weight control or to reduce the risk of non-communicable diseases | Science Media Centre; [consultado el 3 de julio de 2023]. Disponible en: https://bit.ly/49l6Yqo
Yin J, Zhu Y, Malik V, Li X, Peng X, Zhang FF, Shan Z, et al. Intake of Sugar-Sweetened and Low-Calorie Sweetened Beverages and Risk of Cardiovascular Disease: A Meta-Analysis and Systematic Review. Adv Nutr. 2021 Feb 1;12(1):89-101. doi: 10.1093/advances/nmaa084
Diaz C, Rezende LFM, Sabag A, Lee DH, Ferrari G, Giovannucci EL, Rey-Lopez JP. Artificially Sweetened Beverages and Health Outcomes: An Umbrella Review. Adv Nutr. 2023 Jul;14(4):710-717. doi: 10.1016/j.advnut.2023.05.010. Epub 2023 May 13. PMID: 37187453.
Rios-Leyvraz M, Montez J. Health effects of the use of non-sugar sweeteners: a systematic review and meta-analysis. Geneva: World Health Organization; 2022. Licence: CC BY-NC-SA 3.0 IGO. Disponible en: https://www.who.int/publications/i/item/9789240046429
Shea BJ, Reeves BC, Wells G, Thuku M, Hamel C, Moran J et al. AMSTAR 2: a critical appraisal tool for systematic reviews that include randomised or non-randomised studies of healthcare interventions, or both. BMJ. 2017 Sep 21;358:j4008. doi: 10.1136/bmj.j4008
Aguayo-Albasini JL, Flores-Pastor B, Soria-Aledo V. Sistema GRADE: clasificación de la calidad de la evidencia y graduación de la fuerza de la recomendación [GRADE system: classification of quality of evidence and strength of recommendation]. Cir Esp. 2014 Feb;92(2):82-8. Spanish. doi: 10.1016/j.ciresp.2013.08.002.