Versión 1 - 27/03/22
En prevención primaria, el uso de ácido acetilsalicílico (ASA) reduce de forma marginal la incidencia de eventos cardiovasculares mayores, a expensas de un mayor riesgo de sangrados clínicamente importantes. Dado que el balance riesgo/beneficio no favorece su uso rutinario, la opción de iniciar tratamiento debe ser discutida individualmente en el contexto de toma de decisiones compartidas.
Certeza global en la evidencia: moderada (por imprecisión).
Otro mensaje clave:
No se encontró un efecto diferencial del ASA en relación con edad, género, presencia o no de diabetes, categorías de riesgo cardiovascular y uso de estatinas.
Es importante saber lo que no se conoce
– A la fecha no existe una regla de predicción clínica validada que permita estimar/balancear los beneficios y riesgos del ASA en prevención primaria.
– No se conocen si existen diferencias del efecto de ASA por grupo racial dado que la evidencia disponible corresponde principalmente a población caucásica.
Antecedentes
Los eventos cardiovasculares mayores (MACE, por sus siglas en inglés) de origen aterosclerótico representan la principal causa de muerte a nivel mundial. Se estima que para 2015 murieron a causa de estos eventos 17.7 millones de personas (31% de las defunciones en el mundo), de los cuales 7.4 se atribuyeron a cardiopatía isquémica y 6.7 a ataque cerebrovascular (1).
Colombia sigue la tendencia mundial con un 29.5% de muertes secundarias a MACE. Para 2017 los gastos en salud derivados por la atención de MACE y sus factores de riesgo estaban cerca de los 3.84 mil millones de pesos, y las pérdidas anuales por falta de productividad laboral se estimaron en 2.58 mil millones de pesos (3).
Para MACE existen factores de riesgo modificables (hipercolesterolemia, hipertensión arterial, diabetes, sobrepeso/obesidad, tabaquismo, sedentarismo, exceso de alcohol o baja ingesta de verduras, frutas y grasas saludables) y no modificables (edad, sexo e historia familiar) (4). Estos factores se han integrado en ecuaciones de predicción del riesgo de eventos a 10 años o medición de la salud cardiovascular (5). Dichas herramientas permiten clasificar e informar a pacientes a riesgo de estos eventos (escenario de prevención primaria) sobre la necesidad de implementar cambios en su estilo de vida o iniciar ASA o estatinas (6).
El ASA inhibe irreversiblemente la ciclooxigenasa (COX) 1 y 2 impidiendo la agregación plaquetaria (vía reducción de tromboxano A2), lo que previene el proceso de aterotrombosis. La COX es a su vez responsable de la producción de prostaglandinas protectoras de la mucosa de estómago e intestinos, por lo que la administración de ASA también facilita el sangrado digestivo (7).
Dado su beneficio comprobado en el escenario de prevención secundaria, el ASA ha sido empleado por décadas en esa población para disminuir MACE (8). No obstante, su rol en prevención primaria es debatido dado que ensayos clínicos recientes (9-11) han puesto en duda su beneficio lo que explica las diferencias en las recomendaciones de uso emitidas por varias sociedades científicas (tabla 1) (12-18).
Este Recado reseña una reciente revisión sistemática (RS) con metaanálisis del Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF, por su sigla en inglés) (19) sobre beneficios y riesgos del uso de ASA en prevención primaria para reducir MACE.
Información en la que se basa este Recado
Se presenta una evaluación crítica del estudio realizado por USPSTF (19) identificado por monitoreo periódico de repositorios de información. Esta RS fue seleccionada entre otros estudios similares (20-26) por su vigencia y rigor metodológico. Examina el impacto de ASA en prevención de MACE y cáncer de colon, actualizando recomendaciones previas (2016) e incluyendo un modelo de decisión basado en simulación.
Se extrajeron los datos de eficacia y seguridad de ASA en prevención primaria de MACE provenientes de metaanálisis de ensayos clínicos aleatorizados (ECA) y metaanálisis de datos de pacientes individuales (IPD MA, por sus siglas en inglés). Los estudios incluidos en la RS evaluaron el consumo regular de ASA (mínimo 75 mg/día por al menos 12 meses) comparado con placebo o no tomarla. Se excluyeron estudios en los que su uso fuera analgésico o como tratamiento adicional a otros antitrombóticos, incluida warfarina.
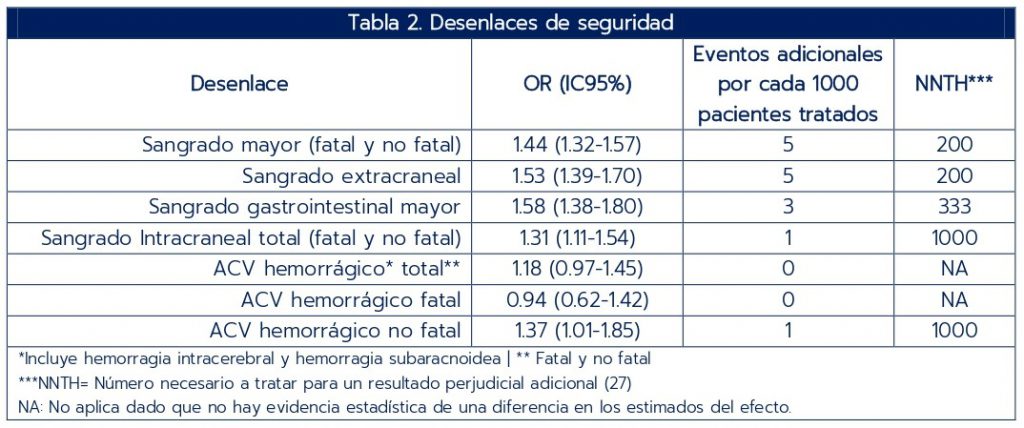
Como desenlaces de eficacia se consideraron infarto de miocardio (IAM) o ataque cerebrovascular (fatal o no fatal), muerte por todas las causas y un compuesto de MACE. Los desenlaces de seguridad fueron ataque cerebrovascular hemorrágico, hemorragia intracraneal (HIC) y sangrado mayor (que incluye hemorragia gastrointestinal grave) definido como sangrado que requiere transfusión o que causa hospitalización o muerte.
Resultados
El metaanálisis incluyó 13 ensayos clínicos con 161 680 participantes, seguidos por 3.6 a 10.1 años. La edad promedio en cada estudio fue entre 53 y 74 años; 52% eran mujeres y la mayoría (>90%) de origen caucásico con características y riesgo cardiovascular basal variables entre los estudios. Once de los trece estudios administraron dosis bajas de aspirina (≤100 mg/día), los dos restantes emplearon dosis de 325 mg o de 300 a 500 mg/día; 5 estudios emplearon aspirina con cubierta entérica.
Para efectos de este Recado se incluyen los datos con ≤100 mg/día, la dosis más usada y disponible en el país.
Desenlaces de eficacia
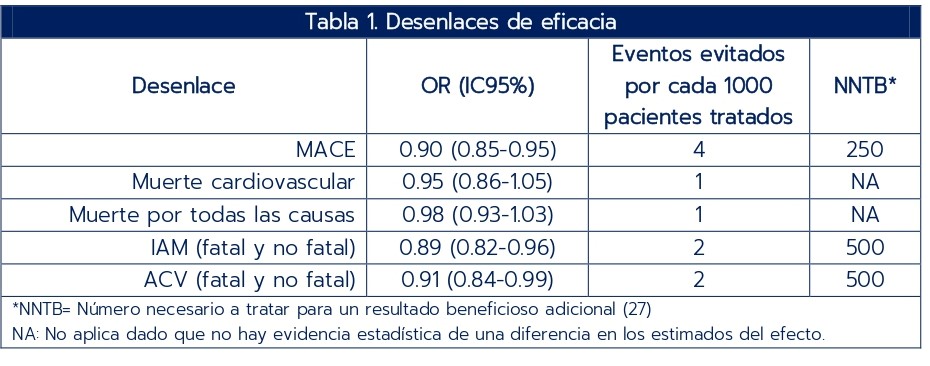 Otros hallazgos
Otros hallazgos
-
-
- No se encontró heterogeneidad en el efecto del tratamiento por grupos de edad. Aunque en los estudios más grandes las pruebas de interacción mostraron un beneficio para edades mayores, los análisis por subgrupos fueron inconsistentes y no mostraron significancia estadística.
- No se encontró un efecto diferencial por sexo o presencia de diabetes.
- La evidencia fue insuficiente para determinar diferencias por el grupo racial.
- Seis estudios estratificaron sus resultados según riesgo cardiovascular (con escalas y umbrales diferentes); cuatro de estos análisis fueron propuestos previamente por los investigadores y cinco realizaron pruebas de interacción sin encontrar diferencias entre grupos.
- El análisis del impacto clínico del ASA en relación con el uso concomitante de estatinas, mostró que después de la publicación de las guías ATP III en 2001 (28) los estudios reportaron una reducción en la incidencia de MACE, IAM y sangrados de relevancia clínica, aunque hubo un incremento en los ACV isquémicos. Sin embargo, estos efectos han sido atribuidos a las dosis altas de aspirina (162.5 mg y 500 mg) en dos grandes estudios (29,30) diferencias en las poblaciones y duración del tratamiento. Tres estudios más recientes ASCEND, ARRIVE y ASPREE no encontraron significancia estadística en las pruebas de interacción entre aspirina y estatinas en sus análisis por subgrupos.
-
Desenlaces de seguridad
Información sobre la evidencia que soporta este Recado
Luego de aplicar la herramienta AMSTAR 2 se concluye confianza alta en los resultados de la RS. Además, la calificación de la calidad de los estudios individuales, basada en la herramienta del USPSTF que califica la validez interna en tres niveles (buena, aceptable o pobre) (25), osciló para los autores de esta RS entre aceptable y buena (31).
Referencias
Organización Mundial de la Salud. Enfermedades cardiovasculares, mayo 17 de 2017. Consultado en 2022 02 02. Disponible en: https://bit.ly/3wIqnl5
Tsao CW, Aday AW, Almarzooq ZI, Alonso A, Beaton AZ, Bittencourt MS, Boehme AK, Buxton AE, Carson AP, Commodore-Mensah Y, Elkind MSV, 3. Evenson KR, Eze-Nliam C, Ferguson JF, Generoso G, Ho JE, Kalani R, Khan SS, Kissela BM, Knutson KL, Levine DA, Lewis TT, Liu J, Loop MS, Ma J, Mussolino ME, Navaneethan SD, Perak AM, Poudel R, Rezk-Hanna M, Roth GA, Schroeder EB, Shah SH, Thacker EL, VanWagner LB, Virani SS, Voecks JH, Wang NY, Yaffe K, Martin SS; American Heart Association Council on Epidemiology and Prevention Statistics Committee and Stroke Statistics Subcommittee. Heart Disease and Stroke Statistics-2022 Update: A Report From the American Heart Association. 2022 Jan 26:CIR0000000000001052. doi: 10.1161/CIR.0000000000001052.
Escobar GL, Orozco, AM, Nuñez JR, Muñoz FL, Mortalidad por Enfermedades Cardiovasculares en Colombia 1993-2017. Un análisis de las políticas públicas. Salud, Barranquilla [online]. 2020, vol.36, n.3, pp.558-570. Epub Oct 22, 2021. ISSN 0120-5552. https://doi.org/10.14482/sun.36.3.616.12.
Yusuf S, Hawken S, Ounpuu S, Dans T, Avezum A, Lanas F, McQueen M, Budaj A, Pais P, Varigos J, Lisheng L; INTERHEART Study Investigators. Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART study): case-control study. Lancet. 2004 Sep 11-17;364(9438):937-52. doi: 10.1016/S0140-6736(04)17018-9
Lloyd-Jones DM. Cardiovascular risk prediction: basic concepts, current status, and future directions. Circulation. 2010 Apr 20;121(15):1768-77. doi: 10.1161/CIRCULATIONAHA
Matheny M, McPheeters ML, Glasser A, Mercaldo N, Weaver RB, Jerome RN, Walden R, McKoy JN, Pritchett J, Tsai C. Systematic Review of Cardiovascular Disease Risk Assessment Tools [Internet]. Rockville (MD): Agency for Healthcare Research and Quality (US); 2011 May. Report No.: 11-05155-EF-1.
Awtry EH, Loscalzo J. Aspirin. Circulation. 2000 Mar 14;101(10):1206-18. doi: 10.1161/01.cir.101.10.1206
Antithrombotic Trialists' Collaboration. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ. 2002 Jan 12;324(7329):71-86. doi: 10.1136/bmj.324.7329.71
Gaziano JM, Brotons C, Coppolecchia R, Cricelli C, Darius H, Gorelick PB, Howard G, Pearson TA, Rothwell PM, Ruilope LM, Tendera M, Tognoni G; ARRIVE Executive Committee. Use of aspirin to reduce risk of initial vascular events in patients at moderate risk of cardiovascular disease (ARRIVE): a randomised, double-blind, placebo-controlled trial. 2018 Sep 22;392(10152):1036-1046. doi: 10.1016/S0140-6736(18)31924-X.
xxxASCEND Study Collaborative Group, Bowman L, Mafham M, Wallendszus K, Stevens W, Buck G, Barton J, Murphy K, Aung T, Haynes R, Cox J, Murawska A, Young A, Lay M, Chen F, Sammons E, Waters E, Adler A, Bodansky J, Farmer A, McPherson R, Neil A, Simpson D, Peto R, Baigent C, Collins R, Parish S, Armitage J. Effects of Aspirin for Primary Prevention in Persons with Diabetes Mellitus. N Engl J Med. 2018 Oct 18;379(16):1529-1539. doi: 10.1056/NEJMoa1804988.
McNeil JJ, Wolfe R, Woods RL, Tonkin AM, Donnan GA, Nelson MR, Reid CM, Lockery JE, Kirpach B, Storey E, Shah RC, Williamson JD, Margolis KL, Ernst ME, Abhayaratna WP, Stocks N, Fitzgerald SM, Orchard SG, Trevaks RE, Beilin LJ, Johnston CI, Ryan J, Radziszewska B, Jelinek M, Malik M, Eaton CB, Brauer D, Cloud G, Wood EM, Mahady SE, Satterfield S, Grimm R, Murray AM; ASPREE Investigator Group. Effect of Aspirin on Cardiovascular Events and Bleeding in the Healthy Elderly. N Engl J Med. 2018 Oct 18;379(16):1509-1518. doi: 10.1056/NEJMoa1805819.
United States Preventive Services Task Forces (USPSTF). Aspirin Use to Prevent Cardiovascular Disease and Colorectal Cancer: Preventive Medication. April 11, 2016. Disponible en: https://bit.ly/3Llj2fj
Piepoli MF, Hoes AW, Agewall S, Albus C, Brotons C, Catapano AL, Cooney MT, Corrà U, Cosyns B, Deaton C, Graham I, Hall MS, Hobbs FDR, Løchen ML, Löllgen H, Marques-Vidal P, Perk J, Prescott E, Redon J, Richter DJ, Sattar N, Smulders Y, Tiberi M, van der Worp HB, van Dis I, Verschuren WMM, Binno S; ESC Scientific Document Group. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts)Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Eur Heart J. 2016 Aug 1;37(29):2315-2381. doi: 10.1093/eurheartj/ehw106
National Institute for Health and Care Excellence Clinical Knowledge Summaries. Antiplatelet treatment: Primary prevention of CVD Last revised September 2018 https://bit.ly/3iEqGVE
American Academy of Family Physicians. Clinical Preventive Service Recommendations: Aspirin Use to Prevent CVD and Colorectal Cancer. https://www.aafp.org/patient-care/clinicalrecommendations/all/aspirin-use-prevention.html.
Scottish Intercollegiate Guidelines Network (SIGN). Risk estimation and the prevention of cardiovascular disease. SIGN Publication No. 149. 2017;2019(Nov 7)
Arnett DK, Blumenthal RS, Albert MA, Buroker AB, Goldberger ZD, Hahn EJ, Himmelfarb CD, Khera A, Lloyd-Jones D, McEvoy JW, Michos ED, Miedema MD, Muñoz D, Smith SC Jr, Virani SS, Williams KA Sr, Yeboah J, Ziaeian B. 2019 ACC/AHA Guideline on the Primary Prevention of Cardiovascular Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. 2019 Sep 10;140(11):e596-e646. doi: 10.1161/CIR.0000000000000678.
American Diabetes Association. Addendum. 10. Cardiovascular Disease and Risk Management: Standards of Medical Care in Diabetes-2020. Diabetes Care 2020;43(Suppl. 1):S111-S134. Diabetes Care. 2020 Aug;43(8):1977-1978. doi: 10.2337/dc20-ad08.
Guirguis-Blake JM, Evans CV, Perdue LA, Bean SI, Senger CA. Aspirin Use to Prevent Cardiovascular Disease and Colorectal Cancer: An Evidence Update for the U.S. Preventive Services Task Force. Evidence Synthesis No. 211. Rockville, MD: Agency for Healthcare Research and Quality; 2021. AHRQ publication no. 21-05283-EF-1. Disponible en: https://bit.ly/3wHt3iR
Barbarawi, M., Kheiri, B., Zayed, Y. et al. Aspirin Efficacy in Primary Prevention: A Meta-analysis of Randomized Controlled Trials. High Blood Press Cardiovasc Prev 26, 283–291 (2019). https://doi.org/10.1007/s40292-019-00325-5
Zheng SL, Roddick AJ. Association of Aspirin Use for Primary Prevention With Cardiovascular Events and Bleeding Events: A Systematic Review and Meta-analysis. 2019 Jan 22;321(3):277-287. doi: 10.1001/jama.2018.20578.
Upadhaya S, Madala S, Baniya R, Saginala K, Khan J. Impact of acetylsalicylic acid on primary prevention of cardiovascular diseases: A meta-analysis of randomized trials. Eur J Prev Cardiol. 2019 May;26(7):746-749. doi: 10.1177/2047487318816387
Abdelaziz HK, Saad M, Pothineni NVK, Megaly M, Potluri R, Saleh M, Kon DLC, Roberts DH, Bhatt DL, Aronow HD, Abbott JD, Mehta JL. Aspirin for Primary Prevention of Cardiovascular Events. J Am Coll Cardiol. 2019 Jun 18;73(23):2915-2929. doi: 10.1016/j.jacc.2019.03.501
Christiansen M, Grove EL, Hvas AM. Primary Prevention of Cardiovascular Events with Aspirin: Toward More Harm than Benefit-A Systematic Review and Meta-Analysis. Semin Thromb Hemost. 2019 Jul;45(5):478-489. doi: 10.1055/s-0039-1687905.
Moriarty F, Ebell MH. A comparison of contemporary versus older studies of aspirin for primary prevention. Fam Pract. 2020 Jul 23;37(3):290-296. doi: 10.1093/fampra/cmz080.Nudy M, Cooper J, Ghahramani M, Ruzieh M, Mandrola J, Foy AJ. Aspirin for Primary Atherosclerotic Cardiovascular Disease Prevention as Baseline Risk Increases: A Meta-Regression Analysis. Am J Med. 2020 Sep;133(9):1056-1064. doi: 10.1016/j.amjmed.2020.04.028.
Masson G, Lobo M, Masson W, Molinero G. Aspirin in primary prevention. Meta-analysis stratified by baseline cardiovascular risk. Arch Cardiol Mex. 2020;90(3):293-299. doi: 10.24875/ACM.20000267.
Schünemann HJ, Vist GE, Higgins JPT, Santesso N, Deeks JJ, Glasziou P, Akl EA, Guyatt GH. Chapter 15: Interpreting results and drawing conclusions. In: Higgins JPT, Thomas J, Chandler J, Cumpston M, Li T, Page MJ, Welch VA (editors). Cochrane Handbook for Systematic Reviews of Interventions version 6.3 (updated February 2022). Cochrane, 2022. Available from training.cochrane.org/handbook.
Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults. Executive Summary of The Third Report of The National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, And Treatment of High Blood Cholesterol In Adults (Adult Treatment Panel III). JAMA. 2001 May 16;285(19):2486-97. doi: 10.1001/jama.285.19.2486
Steering Committee of the Physicians' Health Study Research Group. Final report on the aspirin component of the ongoing Physicians' Health Study. N Engl J Med. 1989 Jul 20;321(3):129-35. doi: 10.1056/NEJM198907203210301
Peto R, Gray R, Collins R, Wheatley K, Hennekens C, Jamrozik K, Warlow C, Hafner B, Thompson E, Norton S, et al. Randomised trial of prophylactic daily aspirin in British male doctors. Br Med J (Clin Res Ed). 1988 Jan 30;296(6618):313-6. doi: 10.1136/bmj.296.6618.313
S. Preventive Services Task Force. U.S. Preventive Services Task Force Procedure Manual. Rockville, MD: U.S. Preventive Services Task Force; 2015. https://bit.ly/37VwVlU